
EGTA溶液は実験室でも頻繁に使用される試薬です。EGTAはethylene glycol tetraacetic acidの略でエチレングリコール四酢酸です。似たような試薬としてEDTAがありますが、どちらもキレート剤として使用され。自分は実際にはカルシウムのキレート剤として使用していました。
作り方だけ知りたい人はEGTA溶液 pH8.0の作り方に飛んでください
EGTAとEDTAの違い
EGTAとEDTAを比較すると以下の表のようになるかと思います。ポイントはEGTAはCaに対して選択性が高い、ということだと思います。
| EGTA | EDTA | |
| 分子量 | 380.35g/mol | 292.2438 g/mol |
| 化学式 | C14H24N2O10 | C10H16N2O8 |
| 構造式 | 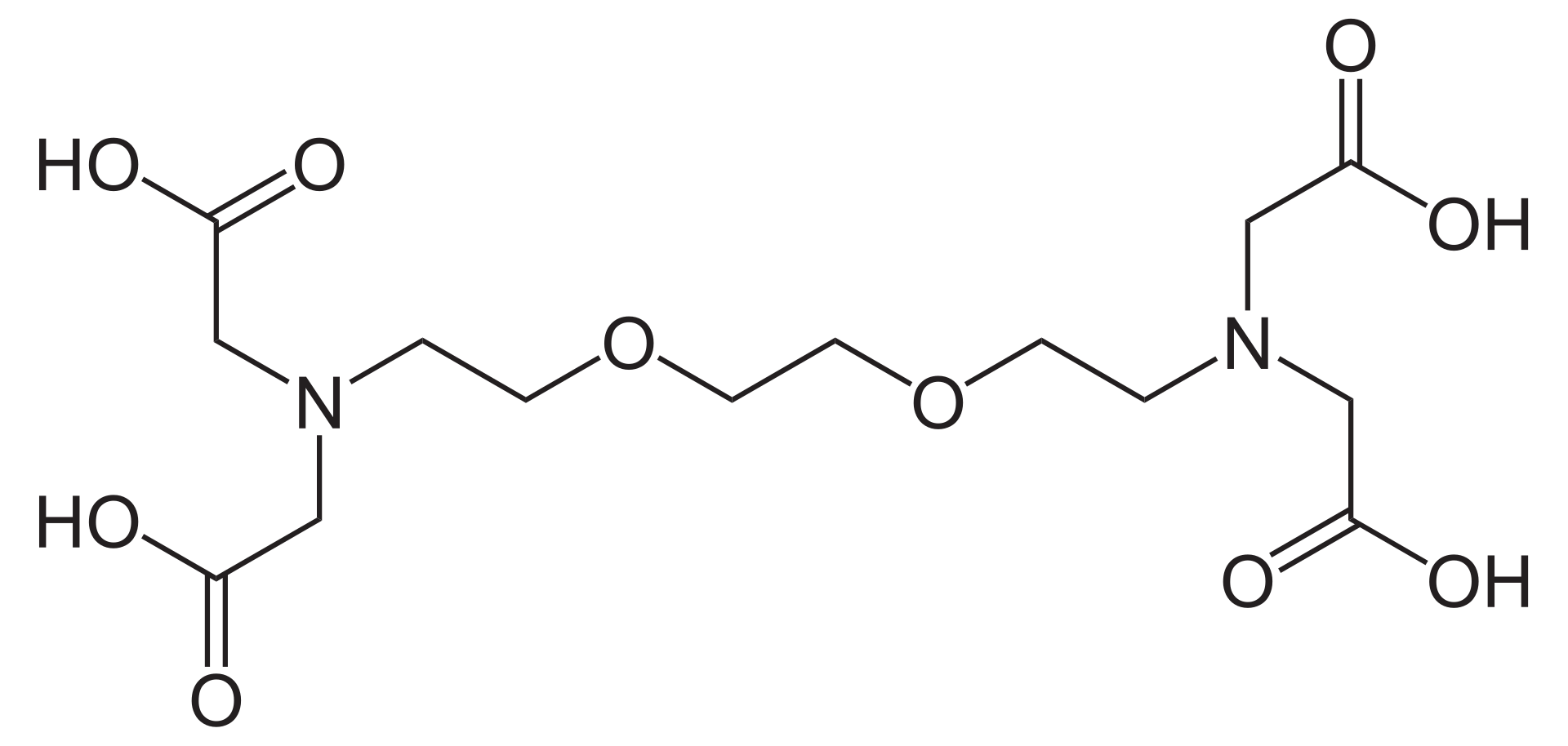 by wikipedia | 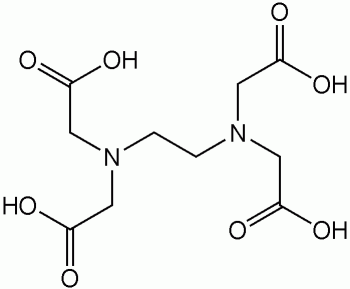 by Wikipedia |
| 選択性 | 特にCa2+, Cd2+に対して選択性高い | Ag+, Ca2+, Mg2+, Cu2+, Fe3+, Zr4+など |
| 溶解度 | <3.8mg/mL in DMSO 水やエタノールに溶けにくい | 0.05g/100mL in H2O 水やエタノールにほとんど溶けない Na塩などではもう少し溶ける |
| 価格 | ¥22500/100g* | ¥9000/500mL (0.5M pH8.0)* |
重要:EGTAはそのままでは水に溶けません
EGTAをそのまま溶かしていくと徐々に水溶液が酸性になるのですぐに溶けなくなります。一方でNaOHを加えてアルカリ性にしていくと溶ける。実際のところあまり原理については詳しくないのですが、化学に詳しい方はもっと詳しく説明できると思います。
500mM EGTA溶液 pH8.0の作り方
準備するもの
- EGTA19g
- ミリQ 水 80mL
- NaOH(顆粒でも水溶液でも)
- ビーカー 100mL作るなら200mLがよい、溢れたり飛び散ったりするため
- メスシリンダー、100mL作るならでいいと思う、メスアップ用
- リトマス紙などのpH試験紙もしくはpH測定できる機械
- スターラーはあると便利
手順
- EGTA19gを測ってビーカーへ
- ミリQ 80mL入れる、この時点では溶けない
- スターラーを投入し混ぜる
- NaOHを少しずつ投与、酸性の状態では溶けないはずなので、色が薄くなったら慎重に入れる。
- pH測定器があれば測定しながらNaOHを投与できる。pHが上がり始めたら一気に8近くまで上昇するので注意。そうも行かない場合は、色が透明になってきてからリトマス紙でチェック、色は勘で判断する
- pH8.0になっていればメスシリンダーに移し、100mLまでミリQ をいれメスアップ
- オートクレーブ後は室温保存でOK、すぐ使い切るならオートクレーブは省略していました


コメント